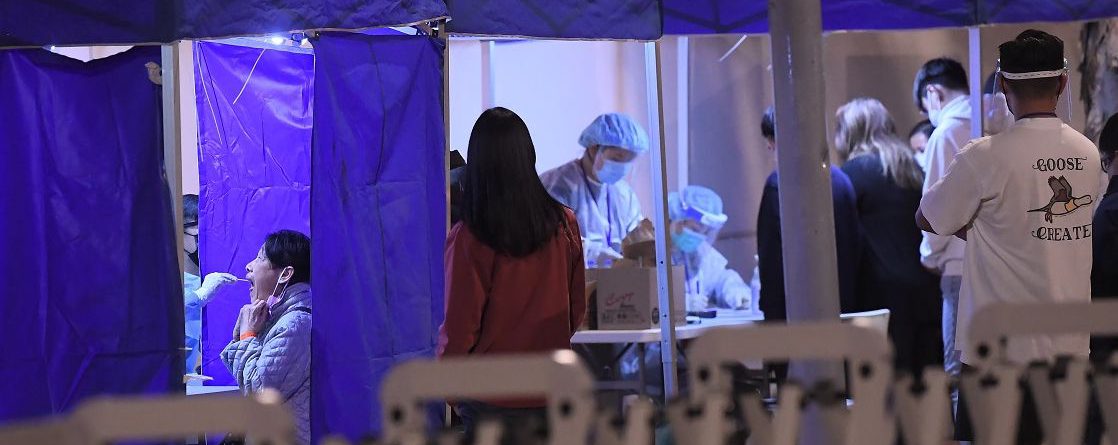
国家卫健委已成立约9000人的采样队,随时来港支援
商务及经济发展局发言人今日(27日)表示,由局长邱腾华负责统筹的医疗物资保障工作小组,在过去一星期已迅速将内地供应的医疗物资分发,供前线人员,以及接受治疗和有需要人士使用。 发言人表示,在中央政府全力支持下,工作小组与内地专班紧密对接,取得很大成果。就特区政府提出的各种医疗物资的需求,包括快速抗原测试包、口罩、中成药、保护装备、医疗用品已陆续分批运抵本港。 截至今日,工作小组已接收约1400万个快速抗原测试包,除部分预留作「全民强制检测」之用,其中约700万个测试包已透过相关部门,向指定高风险及特定群组派发,例如安老院及残疾人士院舍员工及院友、医护人员、清洁工人、跨境货车司机等。另外,民政事务总署已透过「全港社区抗疫连线」,将180万个快速抗原测试包派发予各区市民。 另外,工作小组至今已接收约1100万个N95及KN95口罩。该批口罩主要预留作「全民强制检测」时供市民使用,以加强保护。小组亦已将其中约50万个口罩分发予卫生署及纪律部队前线人员使用。 工作小组亦已接收由内地供应约20万部夹指式脉搏血氧仪,并已全数分发予卫生署及医管局供病人使用。 此外,连同下星期一抵港的批次,工作小组至今共接收35万盒由国家捐赠的抗疫中成药。其中7万盒及5万盒中成药,已分别给予「全港社区抗疫连线」及其他热心社团在社区派发。 其余的23万盒药物将透过相关部门,分发给在医管局辖下18间中医诊所接受治疗的人士及在隔离设施的确诊患者等,让有需要的市民尽快获得这些中央捐赠的中成药,齐心抗疫。 商经局指,工作小组会继续统筹各抗疫部门和单位的医疗物资需求,确保物资能尽快供港作防疫抗疫之用,以全力应对疫情。